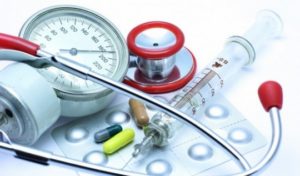
Требования обязывают изготовителей медицинских изделий высоких классов риска, в том числе стерильных медицинских изделий, внедрить систему менеджмента качества и определяют основные характеристики этих систем. Для контроля за выполнением Требований будет проводиться оценка системы менеджмента качества медицинских изделий путем первичного, периодического (планового) и внепланового инспектирования производства. В документе указаны основания для проведения таких инспектирований. Изготовителям медицинских изделий созданы максимально комфортные условия для перехода к работе в новых условиях. С этой целью, а также для формирования перечня инспектирующих организаций Совет ЕЭК установил годовой переходный период с даты вступления этого решения в силу.
Источник: http://pharmnews.kz
Фото: Rosirf
 Мы в Facebook
Мы в Facebook